Fragenteil
Pinned to
211
0
0
No tags specified
|
|
Created by Akram Ben Dhia
almost 9 years ago
|
|
|
|
Copied by b990462
almost 9 years ago
|
|
Close
|
|
Created by Akram Ben Dhia
almost 9 years ago
|
|
|
|
Copied by b990462
almost 9 years ago
|
|

Wie viele Hauptsätze gibt es in der Thermodynamik?
Erläutern Sie folgende Begriffe und nennen Sie jeweils 2 Beispiele:Prozessgröße, Intensive Zustandsgroße, Extensive Zustandsgröße
Definition eines Offenen Systems + Beispiel
Definition eines geschlossenen Systems + Beispiel
Definition eines abgeschlossenen Systems + Beispiel
Erklären Sie mit Hilfe dreier Systeme A, B und C den Nullten Hauptsatz der Thermodynamik.
Geben Sie den 1. Hauptsatz für ein geschlossenes System in differenzieller und in integraler Form an. Es tritt Volumenänderungsarbeit und eine Wärme auf.
Was ist die zentrale Zustandsgröße im Zweiten Hauptsatz der Thermodynamik? Wie kann sie sich in einem abgeschlossenen System ändern?
Was bezeichnen die Ihnen bekannten drei Koeffizienten und wie lautet der Zusammenhang zwischen ihnen?
Stellen Sie das totale Differenzial für die innere Energie U=U(S,T) auf
Zeichen Sie einen Kreisprozess in das p,v-Diagramm ein. Was gilt hierbei für jede Zustandsgröße Z?
Wovon hängt die innere Energie U idealen Gases ab?
Geben Sie die Gleichung für die Entropieänderung eines geschlossenen Systems in differenzieller Form an.
Geben Sie den Inhalt des Dritten Hautsatzes der Thermodynamik wieder.
Nennen Sie die Besonderheiten der kanonischen Zustandsgleichung. Von welchen Größen hängt die kanonische Form der inneren Energie U ab?
Wie sind die freie Energie und die Freie Enthalpie Definiert?
Skizzieren Sie die Phasenübergänge von Wasser und von Kohlenstoffdioxid jeweils qualitativ in einem p,T-Diagramm. Kennzeichnen und beschriften Sie den Tripelpunkt, den kritischen Punkt sowie alle auftretenden Phasengebiete.
Wie lauten die thermische Zustandsgleichung und die kalorische Zustandsgleichung in allgemeiner Form?
Geben Sie die Formel der Gibbsschen Phasenregel an. Benennen Sie dabei die einzelnen Größen.
Nennen Sie die Annahmen, die bei der Betrachtung eines idealen Gases getroffen werden.
Beschreiben Sie für ein ideales Gas folgende Zusammenhänge (Formel):
1) Änderung der spezifischen inneren Energie in Abhängigkeit von der Temperaturänderung bei konstantem Volumen
2) Änderung der spezifischen Enthalpie in Abhängigkeit von der Temperaturänderung bei konstantem Druck
Wie ist der Dampfgehalt definiert? Welchen Wert nimmt der Dampfgehalt auf der Siedelinie an, welchen auf der Taulinie?
Wie wird eine Zustandsgleichung mit Potentialeigenschaften genannt? Erläutern sie diese Eigenschaften.
Von welchen Zustandsgroßen hängt innere Energie bzw. Enthalpie ab, wenn diese in der kanonischen Form gegeben sind?
Wie sind die Größen Cp und Cv definiert?
Wie ist der thermische Wirkungsgrad nth eines Kreisprozesses definiert? Was ergibt sich für einen Carnot-Prozess in Abhängigkeit von Tmin und Tmax?
Geben Sie die Definition der Entropie an.
Wie Lautet der erste Hauptsatz für eine stationären Fließprozess mit zwei Massenströmen (einen eintretenden und einem austretenden), wenn kinetische und potenziale Energieänderungen nicht vernachlässig werden können?
Wie lautet der Zusammenhang zwischen einer individuellen Gaskonstante R, eines idealen Gases und der universale Gaskonstante
Was ist besonderes an einer kanonischen Zustandsgleichung?
Von welchen Zustandsgrößen hängt die freie Enthalpie G ab, wenn sie in der kanonischen Form eingegeben ist?
Skizzieren Sie im p,v-Diagramm die drei Zweiphasengebiete und die Tripellinie! Zeichen Sie auch die kritische Isotherme (Tk), eine Isotherme T1<Tk
Kann eine Temperatur von T=0K erreicht werden? Begründen Sie Ihre Antwort mit Hilfe einer Skizze.
Geben Sie die Gleichung für die Berechnung der Entropieänderung in einem reversiblen Prozess an!
Was entsteht bei einer irreversiblen Zustandsänderung auf Grund der Energiedissipation?
Die kalorische Zustandsgleichung lautet in:
(1) allgemeiner Form
(2) Sonderfall des van der Waals-Medium
(3) Spezialfall des idealen Gases (Cv nicht konstant)
Eine adiabate Expansion findet von p1 auf p2 statt. Stellen Sie die Zustandsänderung für eine reversible adiabate und eine adiabat reibungsbehaftete Änderung in einem T,s-Diagramm dar.
Welche Dimension hat die Volumenänderungsarbeit?
Welche Dimension besitzt der isobare Ausdehnungskoeffizient?
Die Thermische Zustandsgleichung lautet:
allgemeiner Fall
Für ein ideales Gas
Der erste Hauptsatz für ein geschlossenes System lautet in integrale Form:(Erläutern Sie dabei den Typ der auftretenden Grössen)
Geben Sie die Definitionsgleichungen für die Volumenänderungsarbeit und die technische Arbeit an.
Geben Sie die Definitionen der Zustandsfunktionen Enthalpie, freie Energie an:
Wie lautet die thermische Zustandsgleichung nach van der Waals?
Welche physikalische Große wir durch die Konstante b repräsentiert?
Was bedeutet der Korrekturterm
Zeichen Sie in einem T-S-Diagramm jeweils zwei Isobare und zwei Isochore ein und kennzeichnen Sie welche Isobare den höheren Druck und welche Isochore des Größeres Volumen beschreibt.
Wie lautet der erste Hauptsatz U=(S,V) ausgedruckt mit den Zustandsgrößen p, S, V und T?
Wie lautet die kanonische Form der Zustandsgleichungen für U, H, G, und F in differenzielle Schreibweise? Welche Eigenschaften haben alle diese Zustandsgleichungen?
Wie lautet die Gleichung für die Steigung der Dampfdruckkurve?
Für ein ideales Gas sind die Größen

Welcher Term bleibt bei der polytropen Zustandsänderung konstant? Skizzieren Sie in einem p,V-Diagramm jeweils eine isobare, eine isochore, eine reversibel adiabate, eine isotherme und eine polytrope (1<n<k) Zustandsänderung für ein ideales Gas ausgehend vom Zustand 1.
Skizzieren Sie einen Carnot-Prozess in einem T,S-Diagramm. Kennzeichnen Sie die Zustände, die Zustandsänderungen und die abgeführte Wärme. Welchen thermischen Wirkungsgrad hat de Prozess?
Wie ist der Thermische Wirkungsgrad nth eines Kreisprozesses definiert? Was ergibt sich für einen Carnot-Prozess in Abhängigkeit von Tmin und Tmax?
Was besagt das Gibbssche Paradoxon?
Bei der adiabaten Drosselung (stationärer Fließprozess) bleiben folgende Größen konstant:(Fall 1: ideales Gas + Fall 2: realer Gas)
Skizzieren Sie die Joule-Thomson Inversionslinie für ein van der Waals-Gas im dargestellten T(barre),p(barre)-Diagramm. Kennzeichnen Sie die Bereichen der Erwärmung und der Abkühlung sowie die Bereiche, in denen für den isenthalpen Drosselkoeffizienten dh<0,dh=0,dh>0 gilt.
Wie unterscheiden sich Wasserstoff und Stickstoff bei einer adiabaten Drosselung bei 20 °C?
Wie nennt man eine Zustandsänderung eines idealen Gases, bei der sich der Druck umgekehrt proportional zum Volumen verhält?
Welche thermodynamische Zustandsgröße bleibt bei einer adiabaten Drosselung im stationären Fließprozess konstant, wenn kinetische und potenziale Energie vernachlässig werden?Wie verhält sich hierbei die Temperatur im Falle eines idealen Gases?
Wie sind der Molanteil und der Massenanteil eines Gasgemischt definiert? Geben Sie zusätzlich an, wie die isochore spezifische Wärmekapazität eines Gasgemisches bestimmt wird.
Skizzieren Sie in einem p,V sowie T,S-Diagramm einen Carnot-Prozess mit einem idealen Gas. Kennzeichnen Sie die Teilprozesse und zeigen Sie bei welchen Wärme zu- und abgeführt werden.
Einem idealen Gas wir auf drei verschiedenen reversiblen Prozesswegen jeweils die gleiche Wärme Q12 zugeführt. Im Fall A isobar, im Fall B isochor, im Fall C ist der Prozess isotherm. Welche Prozess hat die größte und welcher die kleinste Entropiezunahme? Begründen Sie Ihre Antwort mit Hilfe einer Skizze!
Die Entropieänderung für ein reales Gas bei einer isothermen Zustandsänderung ist definiert als...
Wie verhält sich ein Gas bei adiabaten Drosselung, wenn gilt:
αT<1
αT=1
αT>1
Geben Sie die Definitionen der Zustandsfunktionen Enthalpie, freie Energie, freie Enthalpie und Entropie an.
Von welchen Zustandsgrößen hängt die freie Energie F ab, wenn sie in der kanonischen Form angegeben ist?
Wie lautet die dimensionslöse Form der thermischen Zustandsgleichung für ein Van-der-Waals Gas (bezogen auf die kritischen Größen)? Nennen Sie einen Vorteil dieser Darstellung gegenüber der Formulierung von oben?
Hängt die innere Energie eines van-der-Waals Gases zusätzlich zur Temperatur auch von Volumen ab?
Erläutern Sie den Begriff „Maxwellsche Gerade“. Zeichen Sie hierfür eine p,V-Diagramm.
Was besagt Dalton’sche Hypothese?
Welche thermodynamische Zustandsgröße bleibt bei einer adiabaten Drosselung eines idealen Gases im stationären Fließprozess konstant, wenn kinetische und potenziale Energie vernachlässig werden?
Ein ideales Gas erfährt auf drei verschiedenen reversiblen Prozesswegen jeweils die gleiche Entropiezunahme ΔS. Im Fall A ist der Prozess isobar, im Fall B ist der Prozess isochor, im Fall C ist der Prozess isotherm. Welche Prozess muss hierfür die Größte Wärmemenge Q zugeführt werden und welchem Prozess die kleinste? Begründen Sie Ihre Antwort mittels einer Skizze.
Was ist ein System? Welche verschiedenen Arten von Systemen unterscheidet man?
Was unterscheidet eine Zustandsgröße von einer Prozessgröße? Nennen Sie jeweils ein Beispiel für eine Zustandsgröße und eine Prozessgröße!
Betrachten Sie ein halb voll mit Whisky gefülltes Glas! Nun werfen wir einen Eiswürfel in das Glas! Betrachten wir als System den Whisky mit dem Eis! Handelt es sich hierbei um ein homogenes System?
Warum stellt das erste und das zweite Gleichgewichtspostulat die Grundlage der Temperaturmessung dar?
Welche Werte nimmt die Temperatur 20 °C in der Fahrenheit, Rankine und der thermodynamischen Temperaturskala (Kelvin) an?
Was versteht man unter einer quasistatischen Zustandsänderung?
Nennen Sie jeweils zwei Beispiele von extensiven Zustandsgrößen, intensiven Zustandsgrößen und spezifischen Prozessgrößen!
Wie sind die Größen Enthalpie, freie Energie, freie Enthalpie und Entropie definiert?
Wie groß ist die Volumenänderungsarbeit für eine isobare Zustandsänderung (p=konst), wenn sich das Volumen von V1 auf V2 vergrößert?
Wie groß ist die Volumenänderungsarbeit für eine isochore (
Warum ist p keine extensive Zustandsgröße? Warum ist V eine extensive Zustandsgröße?
G sei eine Zustandsgröße mit der Einheit [J]. Welche Einheit haben dann die Größen g, Gm und G (point)?
Wodurch ist ein adiabates System gekennzeichnet?
Welche physikalischen Effekte müssen bei einer Bilanzierung grundsätzlich berücksichtigt werden?
Existiert eine allgemeingültige und umfassende Definition der thermodynamischen Zustandsgröße „Energie“? Wenn ja, nennen Sie diese; wenn nein, erklären Sie, warum es keine solche Definition gibt!
Sind innere Energie und kinetische Energie Erhaltungsgrößen?
Wie unterscheiden sich bei einem Kolbenverdichter die über einen Arbeitszyklus summierten Volumenänderungsarbeiten von der insgesamt zugeführten technischen Arbeit?
Kann die Entropie eines geschlossenen Systems abnehmen?
Ist es möglich, den absoluten Nullpunkt der Temperatur zu erreichen?
Was versteht man unter dem chemischen Potenzial und in welcher Relation steht es zu der freien Enthalpie?
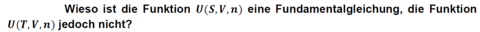
Für welche thermodynamischen Zustandsgrößen bedeutet die Gibbs-Duhem- Gleichung eine Restriktion?
Erläutern Sie den Unterschied zwischen einer Fundamentalgleichung und einer Zustandsgleichung!
Wie lautet die Gibbssche Fundamentalgleichung?
Von welchen Variablen hängt die Fundamentalgleichung der inneren Energie U ab und wie lautet das zugehörige totale Differenzial?
Wie viele Freiheitsgrade hat eine Mischung aus drei Stoffen, bei der zwei verschiedene Phasen auftreten?
Nennen Sie zwei Gründe, warum man mit der Gleichung für das ideale Gas kein reales Verhalten eines Stoffs (z.B. Verflüssigung) beschreiben kann!
Was ist eine Zustandsgleichung? Welche unterschiedlichen Formen von Zustandsgleichungen gibt es?
Leiten Sie aus Gl. (4.9) einen Zusammenhang p(T) für die Dampfdruckkurve her, indem Sie das spezifische Volumen der Flüssigkeit gegenüber dem des Dampfes vernachlässigen und die Verdampfungsenthalpie r=konst. setzen!
Leiten Sie die Beziehung nach Gl. (4.11) her, indem Sie das totale Differenzial des Druckes als Funktion von T und V bilden. Werten Sie diesen Ausdruck dann für p=konst. aus!
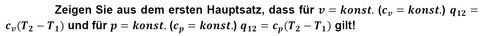

Leiten Sie für einen realen Stoff je eine Beziehung analog zu Gl. (4.51) für die spezifische freie Enthalpie und die spezifische freie Energie aus den Definitionen dieser Größen her!
Warum spricht man davon, dass die van der Waals-Gleichung in reduzierten Variablen einen universellen Charakter hat?
Was versteht man unter van der Waals-Typ-Zustandsgleichungen?
Was beschreibt die Clausius-Clapeyronsche Gleichung?
Welche Zustandsgrößen bleiben jeweils bei einer isobaren, isothermen, isochoren, isenthalpen, reversibel adiabaten und polytropen Zustandsänderung eines idealen Gases konstant?
Welche Zustandsgrößen bleiben jeweils bei einer isobaren, isothermen, isochoren, isenthalpen und reversibel adiabaten Zustandsänderung eines realen Stoffes im Nassdampfgebiet konstant?
Wie groß ist der thermische Wirkungsgrad einer Carnot-Maschine, die zwischen den beiden Temperaturen 1200 K und 300 K betrieben wird?
Eine Carnot-Maschine wird reibungsbehaftet betrieben. Wie ändert sich der thermische Wirkungsgrad und warum?
Was ist leichter: trockene Luft (Luft ohne Wasserdampf) oder feuchte Luft (Luft mit Wasserdampf)? Beide Komponenten (Luft und Wasserdampf) dürfen als ideales Gas behandelt werden.
Betrachten Sie eine adiabate Drosselung in einem mit Gas durchströmten, horizontal liegenden Rohr! Das Gas strömt mit einer hohen Geschwindigkeit durch das Rohr. Wie lautet für diesen Fall der erste Hauptsatz für dieses offene System?
Wie sind der isenthalpe und der isotherme Drosselkoeffizient definiert? Was sagt der isenthalpe Drosselkoeffizient aus?
Was beschreibt die Joule-Thomson Inversionslinie?
Berechnen Sie formelmäßig für eine isenthalpe, adiabate Zustandsänderung im Nassdampfgebiet die umgesetzte spezifische Volumenänderungsarbeit!

Was versteht man unter den Begriffen Exergie und Anergie?
Warum besteht unsere reale Umgebung nicht nur aus Anergie?
Stellen Sie die Nutzarbeit, die einmalig aus einem sehr kalten Gas, das bei Umgebungsdruck vorliegt, bestenfalls gewonnen werden kann, als Fläche in einem p,V-Diagramm dar!
Wie unterscheiden sich Wärmekraftmaschine, Wärmepumpe und Kältemaschine hinsichtlich des jeweils auftretenden Exergiestromes?
Einem Kühlschrank fließt durch Wandwärmeübertragung ein gewisser Energiestrom zu. Wird die Exergie des Kühlraums durch die so gewonnene Energie vergrößert oder verkleinert?
Was versteht man unter dem „schädlichen Raum“ bei einem Kolbenverdichter?
Wie kann man bei Großverdichtern den geförderten Volumenstrom bei konstanter Drehzahl des Antriebsmotors regeln?
Wie ist der isentrope Turbinenwirkungsgrad definiert? Veranschaulichen Sie diesen in einem h,s-Diagramm!
Nennen Sie Beispiele für Arbeitsmaschinen und für Kraftmaschinen! Wie unterscheiden wir diese?
Unter welchen Annahmen können geschlossene und offene Prozesse in gleicher Weise als Kreisprozesse behandelt werden? Was kennzeichnet einen Vergleichsprozess?
Wieso entsprechen die thermischen Wirkungsgrade des Stirling- und des Ericson- Prozesses dem Wirkungsgrad des Carnot-Prozesses?
Welche Maßnahme reduziert bei Dampfkraftprozessen die Erosion der Turbinenbeschaufelung?
Welche fünf verschiedenen Arten von Kälteprozessen kennen Sie, die sich insbesondere durch die unterschiedlichen Formen der zugeführten Antriebsenergie unterscheiden?
In welchem Bereich liegen die typischen Kühlraumtemperaturen für Kaltluft- und Kaltdampfprozesse?
Anhand welcher Kennzahl lassen sich Unter- und Überschallströmungen unterscheiden?
Warum wird bei einer Lavaldüse sowohl der konvergente Kanalteil als auch der divergente Kanalteil als Düse bezeichnet?
Unter welcher Voraussetzung kann in einer Lavaldüse eine Überschallströmung erreicht werden? Wie groß ist dann die Geschwindigkeit an der engsten Stelle der Lavaldüse?
Warum steigt feuchte Luft nach oben?
Warum werden beschlagene Fensterscheiben im Auto ganz schnell frei von ihrem Beschlag, wenn man die Autoklimaanlage einschaltet?
Was versteht man unter der Kühlgrenztemperatur?

 Hide known cards
Hide known cards