Concursos Públicos Biologia Flashcards on QUIMICA RESUMO GERAL, created by Rennan Rizzo on 06/09/2016.
Pinned to
857
12
0
No tags specified
|
|
Created by Rennan Rizzo
about 8 years ago
|
|
Close
|
|
Created by Rennan Rizzo
about 8 years ago
|
|

Se o fenômeno não modifica a composição da matéria, dizemos que ocorre um fenômeno .........
Se o fenômeno modifica a composição da matéria, ou seja, a matéria se transforma de modo a alterar completamente sua composição deixando de ser o que era para ser algo diferente, dizemos que ocorreu um fenômeno ................
Toda mistura é um fenomeno.....
Todo gás é.....
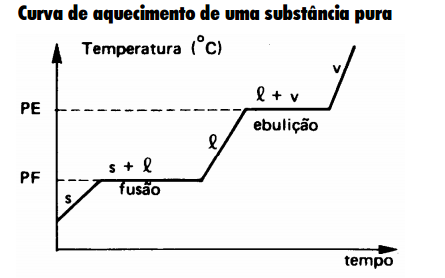
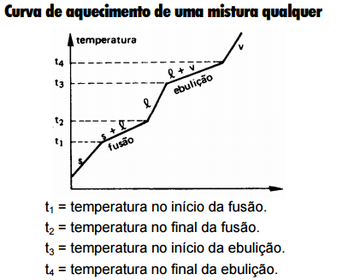
Mistura com Ponto de ebulição constante........
Mistura com PF constante
Separação da agua do ouro
Separação da serragem da areia pela água
separação de sal+areia
O átomo é uma esfera indivisível, indestrutivel e maciça
ATOMOS POSSUEM MASSA IGUAIS
ATOMOS DIFERENTES POSSUEM MASSAS DIFERENTES
FOI CHAMADO DE PUDIM DE PASSAS.
PARA.......... O ÁTOMO ERA UMA ESFERA POSITIVA, NÃO MACIÇA, DIVISIVEL E ELETRICAMENTE NEUTRA
BOMBARDIAMENTO DE UMA RADIAÇÃO EMITIDA PELO POLONIO SOBRE UMA FINA PLACA DE OURO.
A MAIOR PARTE DO ATOMO É ESPAÇO VAZIO(A MAIORIA DAS PARTICULAS ATRAVESSOU A LAMINA.
ATOMO POSSUI UM NUCLEO QUE É POSITIVO. ALGUMAS PARTICULAS RICOCHETEARAM(REPULSÃO)
EXISTEM CARGAS NEGATIVAS GIRANDO AO REDOR DO ATOMO.
A ELETROSFERA É CERCA DE 10000 A 100000 VEZES MAIOR QUE O NUCLEO DO ATOMO
Ao girar ao redor do núcleo, o eletron nao ganha nem perde energia, essas órbitas são níveis estacionarios de energia.
Quando um elétron ganha energia, o mesmo é promovido a um nível mais energético(mais distante do núcleo) e depois retorna ao nivel de origem LIBERANDO ENERGIA EM FORMA DE LUZ(SALTO DE....)
Possuem brilho característico
bons condutores de calor e eletricidade na fase sólida.
São sólidos a temperatura ambiente
São dúcteis
São maleáveis
São cristalinos, solidos na temperatura ambiente
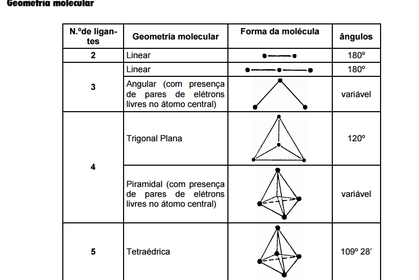
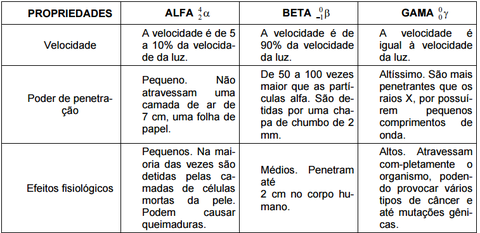
.....é um fenômeno nuclear, o núcleo atomico instavel que emite particulas e radiações, buscando a estabilidade.
Quando um elemento radioativo emite uma partícula alfa
Cada particula......... é um eletron emitido em alta velocidade pelo núcleo radioativo
É formada pela desintegração de um nêutron
Um elemento radioativo emite uma particula beta
É o tempo necessário para que metade dos átomos presentes numa amostra se desintegrem
Na .......... um núcleo muito pesado parte-se e forma núcleos de peso medio
NÃO EXISTEM PARTICULA GAMA!!!!!!!!!!!!!!!!!!!!
O elétron excitado, entretanto, apresenta tendência a retornar ao seu estado natural de 4s1, emitindo um quantum de energia (fóton) quando em seu retorno ao subnível de menor energia,
A segunda lei de Soddy se refere à transformação sofrida pelo núcleo que emite partículas .......
Em uma reação química feita em recipiente fechado, a soma das massas dos reagentes é igual à soma das massas dos produtos.”
Lei de.....
Lei de Conservação da Massa
NO ESTADOS SÓLIDOS AS MOLECULAS ESTÃO BEM PRESAS E SE MOVEM ........
...........é a passagem LENTA da fase líquida para a fase gasosa.
...........é a passagem RÁPIDA da fase líquida para a fase gasosa.
..........são grupos de moléculas iguais. Cada molécula pode ser formada por um grupo de átomos de um mesmo elemento químico ou por elementos diferentes. A água, por exemplo
SANGUE É HETEROGÊNEO
iodo dissolvido em álcool etílico - HOMOGENEO
água /gasolina - HETEROGENEO
gasolina/sal - HETEROGENEO
AGUAL E SAL - HOMOGENEO
(UFMG) Uma amostra de uma substância pura X teve
algumas de suas propriedades determinadas. Todas as
alternativas apresentam propriedades que são úteis para
identificar essa substância, exceto:
a) densidade.
b) massa da amostra.
c) solubilidade em água.
d) temperatura de ebulição.
e) temperatura de fusão.
(Fuvest-SP) Quais das propriedades a seguir são as mais
indicadas para verificar se é pura uma certa amostra sólida
de uma substância conhecida?
a) cor e densidade
b) cor e dureza
c) ponto de fusão e densidade
d) cor e ponto de fusão
e) densidade e dureza
(Vunesp) O rótulo de uma garrafa de água mineral está
reproduzido a seguir.
Composição química provável:
Sulfato de cálcio 0,0038 mg/L
Bicarbonato de cálcio 0,0167 mg/L
Com base nessas informações, podemos classificar a água
mineral como:
a) substância pura.
b) substância simples.
c) mistura heterogênea.
d) mistura homogênea.
e) suspensão coloidal.
As substâncias puras simples são formadas por apenas um elemento químico
exemplo, o gás Nitrogênio
sedimentação fracionada, que nos permitirá separar a
serragem da areia.
sucção
com um pedaço de mangueira introduzido no tanque,
deixando-se escorrer o líquido para um recipiente colocado
no chão. Esse processo é chamado de:
a) decantação c) sifonação
Ao se preparar o tradicional cafezinho, executam-
se dois processos físicos que são, respectivamente:
a) extração e filtração
H3PO4.
Essa substância é composta por:
3 elementos
(PUC-MG) Composição química fixa, densidade, temperatura
constante durante as mudanças de estado físico, pontos
de fusão e ebulição são constantes que caracterizam:
a) mistura azeotrópica d) substância pura
b) mistura heterogênea e) mistura eutética
c) mistura homogênea
O granito consiste em quatro minerais
uma mistura
Água mineral engarrafada, propanona
(C3H6O) e gás oxigênio são classificados, respectivamente,
como:
mistura homogênea, substância pura composta e substância
pura simples.
uma contribuição de Thomson ao modelo atômico,
b) a existência de partículas subatômicas
Eletrosfera é a região do átomo que:
tem volume praticamente igual ao volume do átomo
Segundo Thomson, o átomo seria um aglomerado composto de uma parte de partículas positivas pesadas (prótons) e de partículas negativas (elétrons), mais leves. Este modelo ficou conhecido como “pudim de passas
raios catódicos
Thomson anunciou a existência do elétron, mil vezes menor que o menor átomo conhecido, o do hidrogênio
A justificativa de Mendeleyev foi de que no futuro seriam descobertos novos elementos que preencheriam
esses lugares vazios. De fato, a História provou que ele estava certo
Henry G. J. Moseley estabeleceu o conceito de número atômico, verificando que esse valor caracterizava
melhor um elemento químico do que sua massa atômica
Camada Númeromáximo deelétrons
K 2
L 8
M 18
N 32
O 32
P 18
Q 2
Propriedades periódicas: ocorrem à medida que o número atômico de um elemento químico aumenta, ou seja, assume valores que crescem e decrescem em cada período da Tabela Periódica.
Propriedades aperiódicas:
os valores desta propriedade variam à medida que o número atômico aumenta, mas não obedecem à posição na Tabela

 Hide known cards
Hide known cards